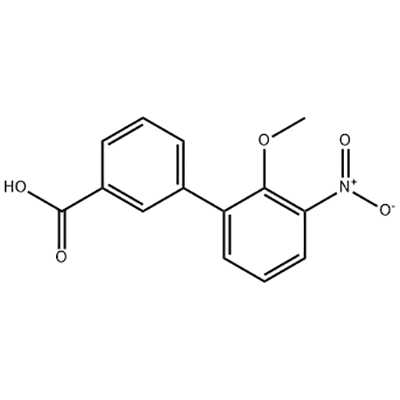
2′-Methoxy-3′-nitro-biphenyl-3-carboxylic acid
2′-Methoxy-3′-nitro-biphenyl-3-carboxylic acid
2'-Methoxy-3'-nitro-biphenyl-3-carboxylic acid د Eltrombopag د منځګړیتوب په توګه کارول کیږي.
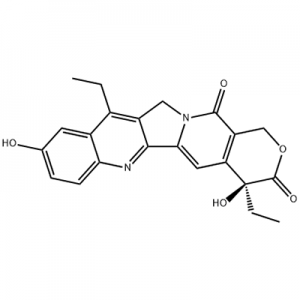
Eltrombopag، په انګلستان کې د GlaxoSmithKline (GSK) لخوا رامینځته شوی او وروسته په سویزرلینډ کې د نووارټیس سره په ګډه رامینځته شوی ، په نړۍ کې لومړی او یوازینی تصویب شوی کوچنی مالیکول غیر پیپټایډ TPO ریسیپټر اګونیسټ دی.Eltrombopag په 2008 کې د متحده ایالاتو FDA لخوا د idiopathic thrombocytopenic purpura (ITP) درملنې لپاره او په 2014 کې د شدید اپلیسټیک انیمیا (AA) درملنې لپاره تصویب شو.دا په تیرو 30 کلونو کې د AA درملنې لپاره د متحده ایالاتو FDA لخوا تصویب شوی لومړی درمل هم دی.
د 2012 په دسمبر کې، د متحده ایاالتو FDA د مزمن هیپاتیت C (CHC) ناروغانو کې د ترومبوسایټوپینیا درملنې لپاره Eltrombopag تصویب کړ، ترڅو د هیپاتیت C ناروغان چې د ټیټ پلیټلیټ شمیرې له امله ضعیف تشخیص ولري د جگر ناروغیو لپاره د انټرفیرون پر بنسټ معیاري درملنه پیل او وساتي.د فبروري په 3,2014 کې، GlaxoSmithKline اعلان وکړ چې FDA د شدید کیمیاوي بک اپلاستیک انیمیا (SAA) ناروغانو کې د هیموپینیا درملنې لپاره د Eltrombopag د بریا درملنې درملو وړتیا ورکړه چې په بشپړ ډول د معافیت درملنې ته ځواب نه ورکوي.د اګست په 24، 2015 کې، د متحده ایاالتو FDA د 1 کالو او تر هغه څخه ډیر عمر لرونکي لویانو او ماشومانو کې د ترومبوسایټوپینیا درملنې لپاره الټرومبوپاګ تصویب کړ چې د اوږدمهاله معافیت ترومبوسایټوپینیا (ITP) سره چې د کورټیکوسټرویډونو ، امونوګلوبولینز یا سپلینکتومي لپاره ناکافي غبرګون لري.د جنوري په 4,2018 کې، Eltrombopag په چین کې د لومړني معافیت ترومبوسایټوپینیا (ITP) درملنې لپاره د لیست کولو لپاره تصویب شو.



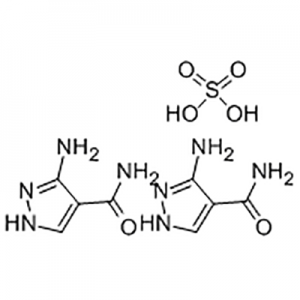
![pentamethylene bis[1-(3,4-dimethoxybenzyl)-3,4-dihydro-6,7-dimethoxy-1H-isoquinoline-2-propionate]، dioxalate](http://cdn.globalso.com/jindunchem-med/image281-300x300.png)

![Casp ungin Acetate؛ Caspofungin Acetate؛ Cancidas؛ Caspofungin Acetate [USAN:BAN:JAN]؛](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)